

Die Arzneimittel stabilität ist eine der kritischsten Herausforderungen in der Pharma industrie. Pharmazeut ische Produkte reichen von chemisch synth etisierten nieder molekularen Arzneimitteln bis hin zu komplexen Bio logika, die von lebenden Organismen oder biotech no logischen Prozessen stammen. Aufgrund ihrer unterschied lichen physikalischen und chemischen Eigenschaften reagieren diese Medikamente sehr unterschied lich auf Temperatur schwankungen.

Bei pharmazeut ischen Tests und Lagerung ist die Temperatur keine Hintergrund bedingung-sie ist ein wichtiger Stabilitäts faktor, der sich direkt auf die Arzneimittel sicherheit,-wirksamkeit und-haltbarkeit auswirkt.
Biologische Medikamente sind aufgrund ihrer protein basierten Strukturen besonders temperature mpfindlich:
Leichte Temperature rhöhungen können zu einer Denaturierung von Proteinen führen
Strukturelle Verformung kann zum Verlust der pharma ko logischen Aktivität führen
Einmal denaturiert, ist die biologische Aktivität oft irreversibel
Selbst geringfügige Temperatur abweichungen während der Prüfung oder Lagerung können die Produkt wirksamkeit beeinträchtigen.
Bei bestimmten flüssigen Zubereitungen können zu niedrige Temperaturen auch Risiken bergen:
Gelöste Stoffe können unter niedrigen Temperatur bedingungen kristallisieren
Konzentration verhältnisse können sich ändern und die Dosierung genauigkeit beeinflussen
Die Kristallisation kann Injektion nadeln blockieren und das Patienten risiko erhöhen
Diese Probleme unterstreichen die Notwendigkeit kontrollierter und wiederholbarer Temperatur umgebungen während der Stabilitäts bewertung.
Medikamente, die für die Langzeit lagerung entwickelt wurden, sind während der Lagerung, des Transports und der täglichen Handhabung kontinuierlich Änderungen der Umgebungs temperatur ausgesetzt. Im Laufe der Zeit können selbst kleine und wiederholte Temperatur zyklen als kumulativer Abbau faktor wirken, was zu:
Chemischer Abbau
Erhöhte Verunreinigung niveaus
Reduzierte therapeut ische Wirksamkeit
Dies macht die Temperatur kontrolle zu einer langfristigen Qualitäts sicherung und nicht nur zu einer kurzfristigen Testa forderung.
Während der frühen Arzneimittel entwicklung ist Unsicherheit unvermeidlich.Temperatur kammernSind wesentliche Werkzeuge für das Formulierung screening und den Stabilitäts vergleich in diesem Stadium.

Typische Anwendungen in Forschung und Entwicklung sind:
Bewertung des Formulierung verhaltens unter hoher und niedriger Temperatur belastung
Simulation von täglichen oder saisonalen Temperatur zyklen
Vergleich der strukturellen Stabilität über mehrere zusammen gesetzte Kandidaten hinweg
Durch die Beobachtung physikalischer und chemischer Veränderungen unter kontrollierten Temperatur bedingungen können Forscher Formulierungen mit stabilen Strukturen und zuverlässiger Leistung identifizieren, die eine solide Grundlage für die weitere Entwicklung bieten.
Test kammer mit hoher niedriger TemperaturBleiben während der gesamten pharmazeut ischen Fertigungs-und Qualitäts sicherungs prozesse unverzicht bar.
Eingehende Rohstoffe werden routinemäßig unter kontrollierten Temperatur bedingungen bewertet. Beispiels weise kann die Qualität der Kapsel gelatine aufgrund von Temperatur unterschieden während der vor geschalteten Verarbeitung variieren. Temperatur kammern helfen zu überprüfen, ob Gelatine eine konstante Gelier leistung sowohl unter Standard-als auch unter extremen Temperatur bedingungen beibehält, bevor sie für die Produktions verwendung zugelassen wird.
In der Antibiotika-Produktion beeinflusst die Fermentation temperatur direkt die Wirkstoff konsistenz. Schon geringe Temperatur abweichungen können zu Chargen variabilität führen. Durch die Simulation verschiedener Fermentation temperatur szenarien in einemKammer mit konstanter Temperatur, Hersteller können:
Analysieren Sie die Auswirkungen der Temperatur auf die Wirkstoff ausbeute
Prozess parameter optimieren
Stellen Sie die Konsistenz von Charge zu Charge sicher
Diese Prozess validierung ist für die Aufrechterhaltung einer stabilen Arzneimittel qualität in großem Maßstab unerlässlich.
Temperatur kammern spielen nach dem Markte in tritt von Medikamenten weiterhin eine wichtige Rolle. Gemäß den regulator ischen Anforderungen führen Pharma unternehmen routinemäßig Stabilitäts studien nach dem Inverkehr bringen unter Verwendung von Markt proben durch.
Diese Studien umfassen typischer weise:
Langzeit exposition unter kontrollierten Lager bedingungen
Periodische Tests auf Verunreinigung wachstum und Potenz verlust
Daten erhebung für die behördliche Inspektion und Prüfung
Wenn Anomalien festgestellt werden, können Hersteller die Speichert mpfeh lungen umgehend anpassen oder Korrektur maßnahmen einleiten, um die Risiken für die Patienten sicherheit zu minimieren.
Die Bewertung der pharmazeut ischen Stabilität stützt sich haupt sächlich auf zwei komplementäre Test ansätze.
Beschleunigte Stabilitäts tests simulieren die langfristige Alterung von Arzneimitteln innerhalb eines kürzeren Zeitraums, indem erhöhte Temperaturen und kontrollierte Feuchtigkeit bedingungen angewendet werden.
Typische Ziele sind:
Vorhersage potenzieller Degradation pfade
Schätzung der Haltbarkeit während der frühen Entwicklung
Unterstützung von Formulierungs-Screening-Entscheidungen
Diese Methode verbessert die F & E-Effizienz erheblich und liefert gleichzeitig wertvolle Vorhersage daten.
Langzeit stabilitäts tests zeichnen Echtzeit änderungen unter Bedingungen auf, die nahe an den tatsächlichen Speicher umgebungen liegen. Diese Daten sind unerlässlich für:
Bestimmung der genauen Ablauf daten
Optimierung der Lager-und Transport bedingungen
Unterstützung von behördlichen Einreichungen und Genehmigungen
Pharmazeut ische Stabilitäts studien werden innerhalb gut etablierter regulatori scher Rahmen bedingungen durchgeführt, um Daten zuverlässigkeit und globale Akzeptanz sicher zustellen. Zu den häufig genannten Richtlinien gehören:
ICH Q1A(R2)-Stabilitäts prüfung neuer Arzneimittel substanzen und-produkte
ICH Q1B-Photos tabilitäts prüfung neuer Arzneimittel substanzen und-produkte
GMPAnforderungen an die Umwelt kontrolle und die Rück verfolgbar keit von Daten
Temperatur kammern, die in pharmazeut ischen Tests verwendet werden, müssen stabile Bedingungen, Wiederholbar keit und vollständige Datensätze unterstützen, um diese regulator ischen Erwartungen zu erfüllen.
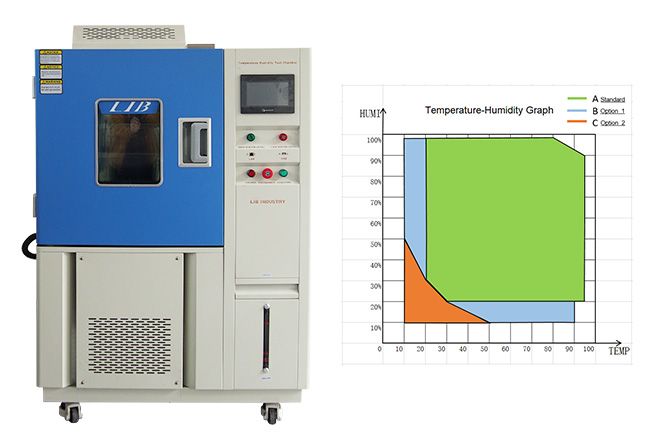
Für pharmazeut ische Stabilitäts tests bieten Temperatur kammern im Allgemeinen die folgenden Leistungs merkmale:
Temperatur bereich:-20 °C bis 60 °C(Anpassbar)
Temperatur schwankung:± 0,5 °C
Temperatur gleichmäßigkeit:± 2 °C
Testmodi: beschleunigte Stabilität und Langzeit stabilität
Daten protokoll ierung: kontinuierliche Aufzeichnung für Audit und Compliance
Diese Parameter gewährleisten konsistente Belichtung bedingungen und zuverlässige Testergebnisse.
Temperatur kammern der LIB-Industrie liefern stabile, wiederholbare Temperatur umgebungen für pharmazeut ische Stabilitäts tests.
Temperatur schwankung: ± 0,5 °C
Temperatur gleichmäßigkeit: ± 2 °C
Unterstützt: beschleunigte und langfristige Stabilitäts studien
Daten protokoll ierung: kontinuierliche Temperatur-und Feuchtigkeit aufzeichnungen
Modell | T-100 | T-225 | T-500 | T-1000 |
Innenraum volumen | 100L | 225L | 500L | 1000L |
Wärme belastung | 1000W | |||
Temperatur bereich | A : -20 ° c ~ 150 B : -40 ° c ~ 150 C: -70 ° c ~ 150 | |||
Temperatur-Schwankung | ± 0,5 ° C | |||
Temperatur abweichung | ± 2,0 ° C | |||
Kühlrate | 1 ° c/min | |||
Heizrate | 3 ° c/min | |||
Kühlsystem | Umwelt freundliches Kältemittel, französischer TECUMSEH-Kompressor, konform mit den Anforderungen der GWP-Standards | |||
Controller | Programmier bare Farbe LCD-Touchscreen-Controller, Ethernet-Verbindung | |||
 | ||||
Diese Funktionen helfen Pharma herstellern, zuverlässige Stabilitäts daten zu generieren, Test abweichungen zu reduzieren und die behördlichen Inspektions anforderungen mit Zuversicht zu erfüllen.
LIB-Industrie temperatur kammern unterstützen pharmazeut ische F & E-, Fertigungs-und Post-Marketing-Stabilitäts programme, indem sie präzise Temperatur kontrolle und Compliance-orientiertes Design kombinieren. und rück verfolgbare Datensätze-Hersteller schützen Produkt qualität und Patienten sicherheit während des gesamten Produkt lebenszyklus.
Kontaktieren Sie die LIB-IndustrieInquiry@libtestchamber.comUm eine konforme zu erhaltenTemperatur kammerLösung innerhalb von 1 ~ 3 Stunden für pharmazeut ische Stabilitäts tests in F & E-, Produktions-und Stabilitäts programmen.
 English
English русский
русский français
français العربية
العربية Deutsch
Deutsch Español
Español 한국어
한국어 italiano
italiano tiếng việt
tiếng việt ไทย
ไทย Indonesia
Indonesia


