

Stabilitäts tests sind eine grundlegende Voraussetzung in der pharmazeut ischen Entwicklung, um sicher zustellen, dass Arzneimittel stoffe und Fertig produkte während ihrer geplanten Haltbarkeit ihre Sicherheit, Wirksamkeit und Qualität behalten. AStabilitäts kammerBietet eine kontrollierte Umgebung-definiert durch präzise Temperatur-, Feuchtigkeit-und Licht verhältnisse (optional)-, um langfristige, mittlere und beschleunigte Speichers zen arien zu simulieren. Für Pharma hersteller sind diese Kammern nicht nur Test geräte, sondern wesentliche Instrumente für die Einhaltung gesetzlicher Vorschriften, die Risiko minderung und die Sicherung des Produkt lebenszyklus.
Dieser Artikel enthält eine umfassende Aufschlüsse lung der Stabilitäts kammer funktionen, technischen Spezifikationen, Regulierungs standards, Validierung sanford rungen, und warum hochpräzise Systeme-wie sie von der LIB-Industrie entwickelt wurden-eine entscheidende Rolle im pharmazeut ischen Qualitäts management spielen.
Eine Stabilitäts kammer ist ein kontrolliertes Umwelt system, das entwickelt wurde, um konstante Temperatur-und Feuchtigkeit bedingungen im Einklang mit den internat ionalen Standards für pharmazeut ische Stabilitäts tests aufrecht zu erhalten.
 |  |
Typische Leistungs parameter sind:
Temperatur bereich: -20 °C bis + 150 °C (anpassbarer Temperatur bereich)
Temperatur genauigkeit: ± 0,1 °C
Temperatur gleichmäßigkeit: ± 0,5 °C
Luft feuchtigkeit bereich: 20% RH-98 % RH
Feuchtigkeit gleichmäßigkeit: ± 2,5% RH
Systeme sind möglicher weise verfügbar als:
Reach-in Stabilitäts kammern (100-1000 L)
Begehbare Stabilitäts kammern (5 m³-100 m³)
Kunden spezifische Stabilitäts kammern für spezielle pharmazeut ische Verpackungen oder übergroße Lasten
Diese genauen Umwelt parameter gewährleisten wiederholbare, validierte Test bedingungen für feste Dosis formen, injizierbare Substanzen, Impfstoffe, Bio logika und APIs.
Pharmazeut ische Produkte sind Abbau risiken wie Oxidation, Hydrolyse, Photo lyse, polymorphem Übergang und physikalischer Instabilität ausgesetzt. AStabilitäts temperatur Feuchtigkeit kammerHilft zu identifizieren:
Haltbarkeit und Verfalls datum
Lagerung sanford rungen (25 ° C gegenüber 30 ° C gegenüber gekühlten Bedingungen)
Verpackungs tauglichkeit (Blister packungen, HDPE-Flaschen, Fläschchen, Aluminium tuben)
Abbau wege unter Stress Auswirkungen von Feuchtigkeit, Temperatur wechsel und Langzeit exposition
Typische Branchen schmerz punkte sind:
Unerwartete OOS (außerhalb der Spezifikation), verursacht durch schlechte Kammer gleichförmigkeit
Langzeit tests mit 12-36 Monaten erfordern eine hohe Zuverlässigkeit
Prüfungs fehler aufgrund unvollständiger 21 CFR Teil 11-Datenprotokolle
Notwendigkeit einer stabilen Leistung im 24/7 Betrieb
Multi-Condition-Tests, die mehrere Kammern oder große begehbare Räume erfordern
Ein Hoch leistungs system minimiert diese Risiken und stellt die Daten präzision und die Einhaltung gesetzlicher Vorschriften sicher.
Eine Stabilitäts kammer in pharmazeuti scher Qualität enthält mehrere fortschritt liche mechanische und Steuerungs merkmale:
PID-Mikroprozessor-Controller Selbst optimierende Algorithmen Dual-RTD-Sensoren für Genauigkeit SSR/Solid-State-Relais für stabile Leistungs steuerung |  |
Umwelt freundliche Kältemittel Mehrstufige Kühlung für strenge Kontrolle Heißgas-Bypass für glatte Modulation Vibrations arme Scroll kompressoren |  |
Einheitlicher laminarer Luftstrom Hoch effiziente Lüfter, die bei konstanter Drehzahl arbeiten Luft geschwindigkeit 1 ~ 2 mt/s für gleichmäßige Verteilung | 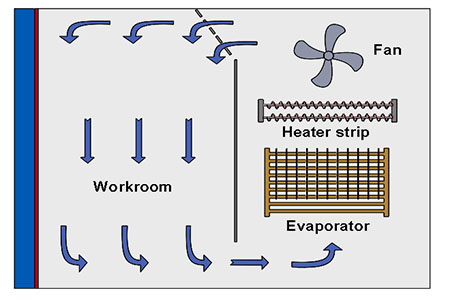 |
304 Edelstahl Innenraum Polyurethan-Schaum isolierung (100mm Dicke) Magnetische Tür dichtungen Optionale Sichtfenster und LED-Beleuchtung |  |
Über temperatur schutz Niedrigwasser-Feuchtigkeit schutz Power-off-Speicher wiederherstellung Türöffnung alarme |  |
Echtzeit-Trend charts USB/Ethernet-Daten export Fern überwachung |  |
Diese mechanischen und digitalen Komponenten gewährleisten langfristige Stabilität und Reproduzier barkeit, insbesondere in mehr monatigen pharmazeut ischen Testprogrammen.
Eine konforme Stabilitäts kammer muss mehrere internat ionale Richtlinien erfüllen. Zu den wichtigsten Standards gehören:
Definiert langfristige, mittlere und beschleunigte Test bedingungen.
Zusätzliche Leitlinien für globale pharmazeut ische Stabilitäts programme.
Verwendet für Impfstoffe, Proteine und Bio logika.
Elektronische Aufzeichnungen & Signaturen für die Daten protokoll ierung.
Europäische Anforderungen und Klimazonen-Klassifikationen.
Kompetenz von Prüf-und Kali brier labors für reproduzierbare Ergebnisse.
Klimazonen (ICH & WHO):
| Zone | Zustand | Anwendung |
| Zone I | 21 °C / 45% RH | Gemäßigt |
| Zone II | 25 °C / 60% RH | Sub tropisch |
| Zone III | 30 °C / 65% RH | Heiß/trocken |
| Zone IVa | 30 °C / 75% RH | Heiß/feucht |
| Zone IVb | 30 °C / 70% RH | Sehr feucht (ASEAN) |
25 °C ± 2 °C / 60% RH ± 5% RH
Dauer: 12-36 Monate
30 °C ± 2 °C / 65% RH ± 5% RH
Dauer: 6-12 Monate
40 °C ± 2 °C / 75% RH ± 5% RH
Dauer: 6 Monate
Eine Stabilitäts kammer muss diese Bedingungen mit extrem geringer Abweichung aufrechterhalten, um genaue und audit fähige Daten sicher zustellen.
Pharmazeut ische Stabilitäts kammern müssen vor der Verwendung validiert werden:
Utility-Check
Nivellierung und Struktur prüfung
Controller-Installation
Komponenten überprüfung
Kalibrierung zertifikate
Temperatur genauigkeit prüfungen
Luft feuchtigkeit genauigkeit tests
Validierung des Alarm-und Sicherheits systems
Überprüfung der Daten protokoll ierung
Volllast-und Leerlast tests
Mapping mit 9-15 Sensoren
72-Stunden-Stabilitäts test
Einheitlichkeit prüfung (± 0,5 °C & ± 2,5% RH typisch)
Die Validierung gewähr leistet einen wiederholbaren, zuverlässigen und konformen Betrieb.
Stabilitäts kammern werden verwendet für:
Tabletten & Capsules Injectables (Fläschchen, Ampullen)
Impfstoffe & Bio logika
Augentropfen & Nasensprays
Verpackungs material prüfung
API-Rohstoffs tudien
Programme zur Verlängerung der Haltbarkeit
Analyse der Verpackungs kompatibilität
Jede Produkt kategorie erfordert eine enge Toleranz und langfristige Betriebs zuverlässigkeit.
Übliche Bedingungen sind 25 ° C/60% RH (langfristig), 30 ° C/65% RH (inter mediär) und 40 ° C/75% RH (beschleunigt).
Kapazität, Temperatur bereich, Feuchtigkeit bereich, Beleuchtung, Regale und Tür design können individuell angepasst werden.
Ja-LIB-Industrie baut Reichweiten kammern und begehbare Stabilitäts räume von 5 m³ bis 100 m³.
In der Regel alle 6-12 Monate, abhängig von SOPs vor Ort und regulator ischen Anforderungen.
Die LIB-Industrie ist auf Präzisions umwelt simulations geräte spezial isiert, die für die Einhaltung von Arzneimitteln entwickelt wurden.
Zu den wichtigsten Vorteilen gehören:
Hohe Genauigkeit: ± 0,1 °C Temperatur/± 1,5% RH
Humidity Einheitlichkeit optimiertes Luftstrom design
Benutzer definierte begehbare Stabilitäts räume bis 100 m³
Zuverlässiger 24/7 Langzeit betrieb
Vollständige Dokumentation: IQ/OQ/PQ + Kalibrierung + Schaltpläne
Globale Installation und Remote-Unterstützung (3 Jahre erweiterte Garantie und lebenslange Service)
LIB-Industrie kammern wurden für einen robusten, kontinuier lichen Betrieb entwickelt und helfen Pharma unternehmen dabei, Audits zu bestehen, OOS-Ereignisse zu reduzieren und die Konsistenz der Produkt qualität sicher zustellen.
Für pharmazeut ische Teams, die ICH-konforme, 21 CFR Part 11 fertige, hochpräzise Stabilitäts lösungen suchen, liefert die LIB-Industrie maßge schneiderte Kammern, die auf langfristige Zuverlässigkeit und globale Einhaltung gesetzlicher Vorschriften ausgelegt sind. Kontaktieren Sie unsInquiry@libtestchamber.comFür Spezifikationen, Anpassungs optionen oder ein formales Angebot.
 English
English русский
русский français
français العربية
العربية Deutsch
Deutsch Español
Español 한국어
한국어 italiano
italiano tiếng việt
tiếng việt ไทย
ไทย Indonesia
Indonesia


